


阿爾茨海默病(Alzheimer’s disease,AD)是一種常見的神經退行性疾病,主要表現為記憶缺失,語言能力下降和認知功能障礙。目前,AD仍然無法治愈,主要歸因于AD發病機理不明确以及對疾病診斷困難。AD的發病機制相關假說及靶點較多,越來越多研究表明Tau蛋白的病理發展與AD的認知功能高度相關。随着納米技術的發展,新型功能材料能夠實現對疾病同時診斷和治療。因此,針對Tau通路構建一個新型的藥物遞送系統用于AD的治療和診斷具有重要研究意義。納米金屬有機框架(Nanoscale Metal Organic Frameworks, NMOFs)因具有多種優勢在生物醫藥領域應用廣泛,如均勻可調的孔徑,高負載能力,可控的藥物釋放動力學和改善的生物相容性等。
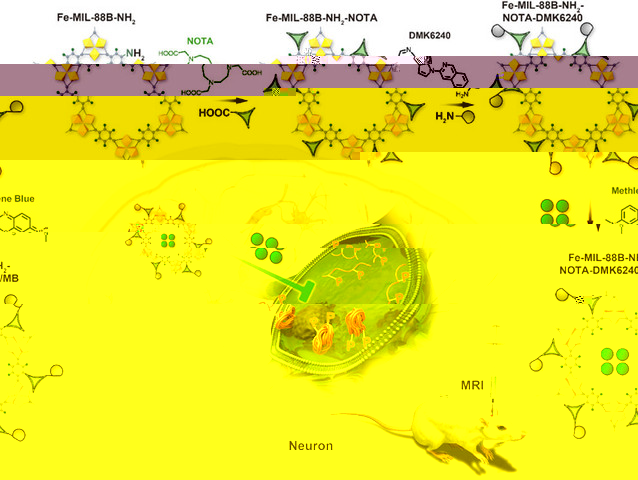
孔令義教授團隊選擇NMOF磁性材料Fe-MIL-88B-NH2為載體,通過酰胺縮合反應在其表面進行功能化修飾,用1,4,7-三氮雜環壬烷-1,4,7-三乙酸(NOTA)将靶向Tau蛋白試劑5-氨基-3-(吡咯并[2,3-c]吡啶-1-基)異喹啉(Defluorinated MK6240,DMK6240)連接于Fe-MIL-88B-NH2表面,用來增強該系統對磷酸化Tau蛋白的靶向作用,最後将Tau蛋白聚集抑制劑——亞甲藍(Methylene Blue,MB)——封裝在該系統中,該系統不僅能遞送藥物,還可作為核磁成像造影劑。通過XRD、IR、TGA、SEM等方法對該體系的組成、形貌等特征進行了表征。通過高内涵、MRI、Morris水迷宮等體内外實驗證明,Fe-MIL-88B-NH2-NOTA-DMK6240是優良的T2加權核磁成像造影劑,Fe-MIL-88B-NH2-NOTA-DMK6240/MB可以像“導彈”一樣定點釋放MB,抑制磷酸化Tau的聚集,保護神經元,最終改善AD的症狀。
(供稿部門:天然藥化系,撰寫人:王小兵)
CopyRight BETVLCTOR伟德唯一官网 - 伟德官网下载客户端 版權所有
地址:江蘇省南京市江甯區BETVLCTOR伟德唯一官网